Длительное применение препарата Афалаза у больных с ДГПЖ: влияние на снижение симптомов и риска прогрессии
Д.Ю. Пушкарь, К.Б. Колонтарев, А.Н. Берников
Введение. Несмотря на достижения современной медицины, доброкачественная гиперплазия предстательной железы (ДГПЖ) остается значимой проблемой среди мужчин. По данным на 2019 г., во всем мире количество зарегистрированных случаев ДГПЖ в период с 2000 по 2019 г. увеличилось на 70,5% (68,6–72,7) [1]. Отсутствие своевременного лечения ДГПЖ приводит к прогрессии заболевания. По мере увеличения объема предстательной железы усиливаются обструктивные и ирритативные симптомы, что неразрывно связано с увеличением количества баллов по шкале IPSS (8 баллов и выше). Прогрессия ДГПЖ повышает риск проведения оперативного или малоинвазивного вмешательства. Возрастает риск возникновения острой задержки мочи (ОЗМ). Необходимость оперативного лечения ОЗМ может быть обусловлена отсутствием возможности катетеризации или ее неэффективностью. У 44,5% пациентов с ДГПЖ ОЗМ является причиной госпитализации [2].
Афалаза – препарат, применяемый для лечения ДГПЖ, а также для предотвращения ее прогрессии и облегчения симптомов заболевания [3].
Действующими компонентами препарата Афалаза являются обработанные по градуальной технологии [4] аффинно очищенные антитела (АТ) к эндотелиальной синтазе оксида азота (eNOs) и аффинно очищенные антитела (АТ) к простатоспецифическому антигену (ПСА). АТ к ПСА модифицируют функциональную активность эндогенного ПСА, оказывают противовоспалительное и противоотечное действие. АТ к eNOs усиливают скорость кровотока, способствуют снижению реактивности сосудов, уменьшению сосудистого спазма и улучшению периферической микроциркуляции. Комбинация действующих веществ препарата Афалаза сопровождается синергическим эффектом: АТ к eNOs за счет эндотелиопротективного действия и улучшения васкуляризации усиливают антипролиферативную и противовоспалительную активность АТ к ПСА.
Исследования показали, что при приеме препарата Афалаза у пациентов наблюдается уменьшение объема предстательной железы, что способствует снижению давления на мочеиспускательный канал, улучшение показателей максимальной скорости потока мочи и уменьшение остаточной мочи.
Клиническая эффективность препарата была подтверждена в двойном слепом плацебо-контролируемом исследовании Д.Ю. Пушкаря и соавт., в котором приняли участие 260 мужчин в возрасте 45–60 лет. Результаты исследования продемонстрировали эффективность препарата не только в предотвращении увеличения объема предстательной железы, но и в улучшении качества жизни. Среднее значение общего балла IPSS в течение 12 месяцев лечения у пациентов из группы препарата Афалаза снизилось с первоначальных показателей в диапазоне от 11,9±1,9 до 7,9±3,0 баллов, в то время как в группе плацебо показатели с 11,4±1,8 снизились до 8,5±2,5 балла. Разница была статистически значимой (p<0,005). Объем предстательной железы уменьшился у мужчин,IPSS До терапиипринимавших препарат Афалаза, на 5,5±8,0 см³ после 12 месяцев лечения по сравнению с 2,5±5,7 см³ в группе плацебо [5].
В многоцентровом исследовании Ю.А. Куприянова и соавт. у пациентов, ранее не получавших лечения, препарат Афалаза также подтвердил свою клиническую эффективность. После 30 недель терапии наблюдалось значительное снижение общего балла IPSS, также было показано уменьшение максимальной скорости потока мочи (Qmax) с 12,7±4,6 до 16,4±5,7, объем простаты уменьшился на 5,15% [6].
Преимущество препарата Афалаза – благоприятный профиль безопасности, лекарственное средство обладает хорошей переносимостью, что делает его препаратом выбора в терапии ДГПЖ.
Оценка действия препарата Афалаза на протяжении длительного периода (более 12 месяцев) является важным аспектом в терапии ДГПЖ. На основе данных наблюдательной программы будет оценена эффективность и безопасность применения препарата. Полученные результаты позволят скорректировать подходы терапевтического лечения ДГПЖ и снизить риск проведения хирургических операций на простате.
Цель исследования. Получение дополнительных данных об эффективности препарата Афалаза при длительном применении у пациентов с ДГПЖ.
Материалы и методы. Дизайн исследования – ретроспективная наблюдательная программа. В исследование были включены данные 99 медицинских карт пациентов.
Критерии включения: установленный диагноз ДГПЖ, возраст старше 40 лет, терапия препаратом Афалаза более года, использование опросника IPSS для оценки симптомов нижних мочевыводящих путей (СНМП), наличие данных трансабдоминального и трансректального ультразвукового исследования, (ТАУЗИ, ТРУЗИ), магнитнорезонансной томографии (МРТ) по объему предстательной железы.
Критерии исключения: медикаментозная терапия СНМП/ДГПЖ (альфа-адреноблокаторы, ингибиторы 5-аредуктазы, фитопрепараты, органотропные препараты, ферменты) до назначения препарата Афалаза, хирургическое лечение ДГПЖ в анамнезе.
Статистический анализ. Статистический анализ был проведен с помощью анализа ANСOVА. Ковариатами выступали возраст, длительность терапии в месяцах и длительность терапии по категориям. Данные представлены в виде M±SD (median, min, max).
Результаты. В исследовании был произведен анализ данных медицинских карт пациентов в возрасте от 42 до 73 лет, средний возраст составил 50,8±6,9 года. Продолжительность лечения препаратом Афалаза варьировалась. 18,2% пациентов принимали препарат в период от одного года до двух лет, 53,5% продолжали терапию от двух до трех лет, а 27,3% получали лечение более трех лет. Также в исследование был включен один пациент (1%), чье лечение длилось 11 месяцев и три недели. Включение этого пациента в программу было обусловлено необходимостью оценки безопасности приема препарата Афалаза. Таким образом, средняя продолжительность приема препарата составила 26 месяцев (26, 11, 41), что позволило оценить эффект препарата в долгосрочной перспективе.
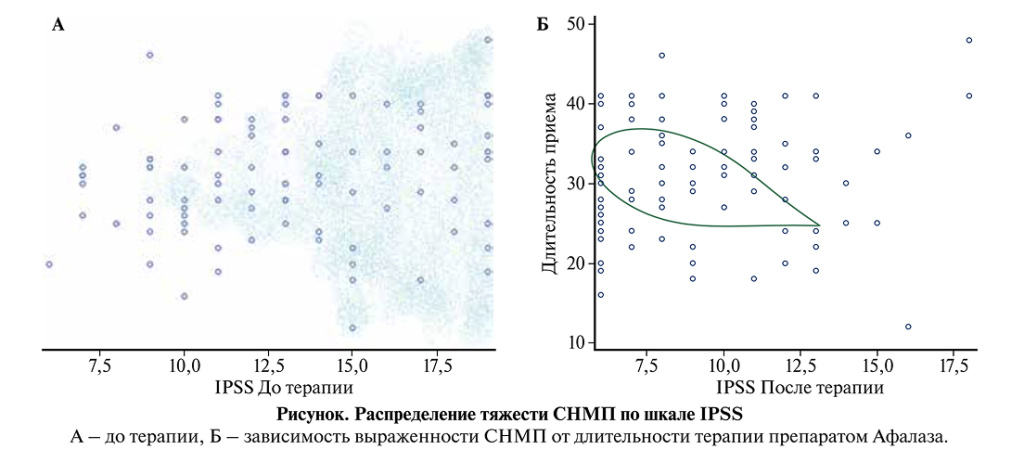
Оценка симптомов по шкале IPSS. До начала терапии средний балл IPSS составил 13,3±3,6 балла (13, 6, 19). После завершения курса терапии наблюдалось снижение среднего показателя по шкале IPSS, до 9,4±3,1 (9, 6, 18). Среднее изменение по шкале IPSS составило 3,8±2,7 балла (4, -6, 9) что является клинически значимым улучшением симптоматики. Изменения по шкале IPSS были статистически значимы (F1/99=203,8, p<0,0001).
Длительность терапии оказала влияние на тяжесть симптомов СНМП (F1/99=8,75, p=0,0039). Была показана прямая зависимость уменьшения выраженности СНМП с увеличением длительностью терапии (рис. 1).
Результаты лечения не зависели от возраста пациентов (F1/99=0,01, p=0,9172).
Изменения объема простаты. До начала терапии средний объем простаты составил 39,9±6,1 см³ (40, 30, 60). После окончания терапии средний объем простаты снизился до 38,0±6,1 см³ (38, 28, 58). Среднее уменьшение объема простаты составило 1,9±1,0 см³. Изменения объема простаты были статистически значимы (F1/99=364,85, p<0,0001). Изменения объема простаты на фоне лечения не было связано ни с возрастом, ни с длительностью терапии. Наблюдения ОЗМ и необходимость хирургического лечения не зарегистрированы. По данным амбулаторных карт, нежелательные явления при приеме препарата Афалаза отсутствовали.
Обсуждение. Результаты ретроспективного исследования подтверждают клиническую эффективность и безопасность длительного применения препарата Афалаза для лечения доброкачественной гиперплазии предстательной железы. Одним из ключевых показателей эффективности терапии является снижение среднего балла по шкале IPSS с 13,3 до 9,4 балла, что свидетельствует о клинически значимом улучшении состояния пациентов и снижении выраженности симптомов заболевания. Препарат проявил свою эффективность независимо от возраста пациентов, что делает его препаратом выбора у мужчин с ДГПЖ различных возрастных групп.
Снижение выраженности симптомов заболевания по шкале IPSS по мере увеличения длительности терапии подчеркивает важность назначения длительного курса препарата Афалаза. Эффект препарата статистически значим (p=0,0039), что позволяет рекомендовать продолжительный прием для достижения максимального терапевтического эффекта. При приеме Афалаза более года нежелательных явлений выявлено не было.
Снижение объема простаты является показателем эффективности препарата. Среднее уменьшение объема предстательной железы на 1,9 см³ подтверждает терапевтический эффект препарата. Уменьшение объема простаты снижает риск прогрессии заболевания и вероятности хирургического лечения ДГПЖ [7].
Заключение. Полученные результаты согласуются с данными предыдущих клинических исследований, в которых также наблюдалось улучшение симптомов нижних мочевыводящих путей, уменьшение объема предстательной железы, снижение риска возникновения ОЗМ во время лечения препаратом Афалаза.
Таким образом, длительное применение препарата Афалаза подтверждает свою эффективность в улучшении качества жизни пациентов с ДГПЖ и может быть рекомендовано для длительного приема с целью предотвращения прогрессии заболевания и хирургического вмешательства.
Афалаза – инновационный препарат, который действует принципиально по-новому и обеспечивает новый подход к патогенетической составляющей ДГПЖ. Представленные результаты составляют предварительные данные. Препарат нуждается в дальнейшем изучении различных групп больных с ДГПЖ, возможно, у пациентов, которым выполнена биопсия простаты при повышении уровня ПСА сыворотки крови и диагностирована гиперплазия простаты и отсутствовал рак простаты.
Список литературы
- GBD 2019 Benign Prostatic Hyperplasia Collaborators. Global, regional, and national burden of benign prostatic hyperplasia, 2000–2019: a systematic analysis for the Global Burden of Disease Study 2019. Lancet Healthy Longev. 2022;3(11):e754-e776. doi: 10.1016/S2666-7568(22)00213-6.
- Apolikhin O.I., Sivkov A.V., Yanenko E.K., Katibov M.I., Zolotukhin O.V., Shaderkin I.A., Prosyannikov M.Y., Voitko D.A., Tsoi A.A., Galiev N.A.,Kastrikin Y.V. Frequency of acute urinary retention as an indicator of quality of medical care for patients with prostatic adenoma. Urologiia. 2016;2:43–48. Russian (О.И. Аполихин, А.В. Сивков, Э.К. Яненко, М.И. Катибов, О.В. Золотухин, И.А. Шадеркин, М.Ю. Просянников, Д.А. Войтко, А.А. Цой, Н.А. Галиев, Ю.В. Кастрикин. Частота выявления острой задержки мочи как индикатор качества оказания медицинской помощи пациентам с аденомой предстательной железы. Урология. 2016;(2):43–48).
- Instructions for the medical use of the drug Afalaza. LP-no. (000021)-(RG-RU)-260422 (electronic resource.) URL: https://grls.rosminzdrav.ru/ (date of access: 08.11.2024). Russian (Инструкция по медицинскому применению препарата Афалаза. ЛП-№ (000021)-(РГ-RU)-260422 (электронный ресурс.) URL: https://grls.rosminzdrav.ru/ (дата обращения: 08.11.2024)).
-
General Pharmacopoeia article of the State Pharmacopoeia of the Russian Federation XV edition of the OFS. 1.7.0001. Biological medicines obtained on the basis of graduated technology. Date of introduction 01.09.2023. (Electronic resource.) URL: https://pharmacopoeia.regmed. ru/pharmacopoeia/izdanie-15/1/1-9/biologicheskie-lekarstvennye- preparaty-poluchennye-na-osnove-gradualnoy-tekhnologii / (date of access: 08.11.2024). Russian (Общая фармакопейная статья Государственной фармакопеи Российской Федерации XV издания ОФС. 1.7.0001. Биологические лекарственные препараты, полученные на основе градуальной технологии. Дата введения 01.09.2023. (Электронный ресурс.) URL: https://pharmacopoeia.regmed.ru/pharmacopoeia/izdanie-15/1/1-9/biologicheskie-lekarstvennye-preparaty-poluchennye-na-osnove-gradualnoy-tekhnologii/ (дата обращения: 08.11.2024)).5. Pushkar D., Vinarov A., Spivak L., Kolontarev K., Putilovskiy M., Andrianova
-
Pushkar D., Vinarov A., Spivak L., Kolontarev K., Putilovskiy M., Andrianova E., Epstein O. Efficacy and safety of Afalaza in men with symptomatic benign prostatic hyperplasia at risk of progression: a multicenter, double-blind, placebo-controlled, randomized clinical trial. Cent European J Urol. 2018;71(4):427-435. doi: 10.5173/ceju.2018.1803.
-
Kupriyanov Y.A., Rasner P.I., Rokhlikov I.M., Akrikidi A.A., Soloviev V.V., Markov A.A., Nozdrin E.V., Logvinov L.A., Vasilevskiy R.P., Skrupskiy K.S., Pushkar D.Yu., Putilovskiy M.A., Epstein O.I. The experience of using drug Afalaza for treatment of lower urinary symptoms in treatment-nave patients with benign prostatic hyperplasia. Urologiia. 2019;(3):36–42. Russian (Куприянов Ю.А., Раснер П.И., Рохликов И.М., Акрикиди А.А., Соловьев В.В., Марков А.А., Ноздрин Е.В., Логвинов Л.А., Василевский Р.П., Скрупский К.С., Пушкарь Д.Ю., Путиловский М.А., Эпштейн О.И. Опыт применения препарата Афалаза для лечения симптомов нижних мочевых путей у пациентов с доброкачественной гиперплазией предстательной железы без предшествовавшей терапии. Урология. 2019;(3):36–42).
-
Clinical recommendations – Benign prostatic hyperplasia – 2020-2021-2022 (01/31/2023) – Approved by the Ministry of Health of the Russian Federation (Electronic resource.) URL:http://disuria.ru/_ld/13/1392_kr20N40MZ.pdf (date of application: 08.11.2024). Russian (Клинические рекомендации – Доброкачественная гиперплазия предстательной железы – 2020-2021-2022 (31.01.2023) – Утверждены Минздравом РФ (Электронный ресурс.) URL:http://disuria.ru/_ld/13/1392_kr20N40MZ.pdf (дата обращения: 08.11.2024)).